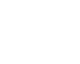Über die Kymos-Gruppe
Die Kymos Group ist eine GLP/GMP-zertifizierte, GCP-konforme, von der EMA, ANVISA und FDA inspizierte europäische Auftragsforschungsorganisation (CRO), die ein umfassendes Angebot an bioanalytischen Dienstleistungen und Qualitätskontrollleistungen für niedermolekulare Wirkstoffe, Biologika und neuartige Therapien anbietet.
Der Kern unseres Seins
Unsere Vision und Mission
Wir setzen uns mit voller Überzeugung für eine positive soziale Wirkung ein, indem wir Vielfalt, Geschlechtergleichstellung, das Wohlbefinden unserer Mitarbeiter, Umweltschutz und soziale Verantwortung fördern.
Unsere Vision ist es, ein erstklassiges CRO & CLO zu sein, das ein umfassendes und innovatives Portfolio an Mehrwertdiensten anbietet, die zur Vermarktung von pharmazeutischen Produkten beitragen und letztendlich den Patienten zugutekommen.
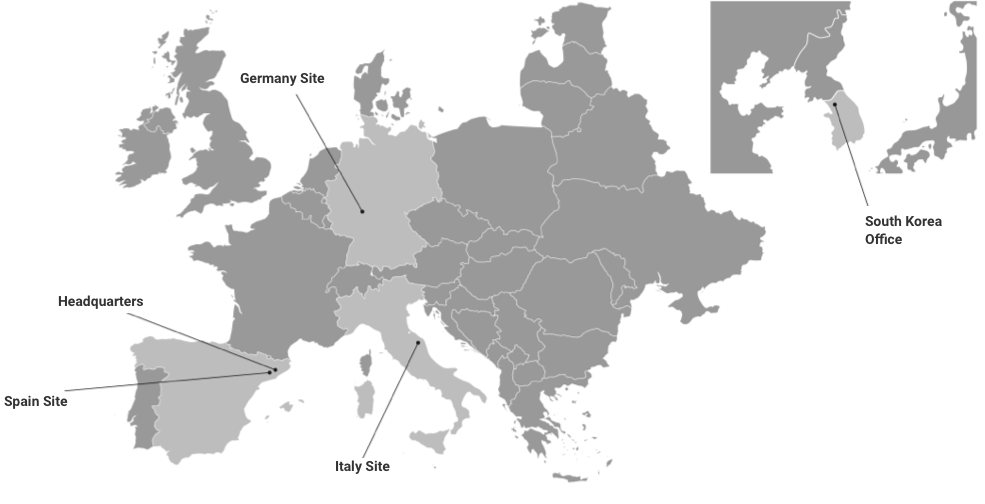
Drei Standorte in Europa – Eine starke Gruppe
Unsere globale Reichweite
Unser Hauptsitz und unser Hauptlabor befinden sich in Barcelona (Kymos Spanien), weitere Labore befinden sich in Frankfurt (Kymos Deutschland, ursprünglich Prolytic) und Ancona (Kymos Italien, ursprünglich Pharmaprogress).
Die Kymos Group engagiert sich für die Unterstützung von Pharma-, Biotech-, Generika- und Biosimilar-Kunden in über 60 Ländern weltweit. Wir helfen ihnen, ihre Produkte zu entwickeln, Kosten zu senken und die Markteinführungszeit zu verkürzen – mit unserem einzigartigen, maßgeschneiderten Ansatz und unserem multidisziplinären Verständnis des gesamten Entwicklungs- und Herstellungsprozesses: von der frühen Forschung und Entwicklung über die Produktentwicklung, die präklinischen und klinischen Phasen bis hin zur endgültigen Zulassung und den Anforderungen nach der Markteinführung .
Kymos Spanien
Kymos SL wurde 2001 in Barcelona von einem Team von F&E-Wissenschaftlern gegründet, die über jahrzehntelange Erfahrung in der pharmazeutischen Entwicklung verfügen – von der frühen Forschung bis zur endgültigen Formulierung und den Scale-up-Studien zur Kommerzialisierung.
- Bioanalyse kleiner Moleküle (auch Massenspektrometrie und Permeationsanalyse genannt)
- Bioanalyse großer Moleküle (auch Immunologie genannt)
- Analytische Entwicklung und Validierung
- Qualitätskontrolle von kleinen Molekülen
- Qualitätskontrolle großer Moleküle (auch bekannt als biopharmazeutische Prüfung)
- Elementaranalyse
- Mikrobiologie
- Stabilitäten
Kymos Deutschland
Die Prolytic GmbH wurde 2002 von erfahrenen Wissenschaftlern der Viatris GmbH, dem größten Geschäftsbereich der Degussa/ASTA Medica AG, gegründet. Das neu gegründete Auftragsforschungsinstitut (CRO) mit Sitz in Frankfurt konzentrierte sich auf die Erbringung bioanalytischer und pharmakokinetischer Dienstleistungen für Kunden der Pharmabranche. 2020 wurde Prolytic Teil der Kymos-Gruppe.
- Bioanalyse kleiner Moleküle (auch Chromatographie genannt)
- Bioanalyse großer Moleküle (auch bekannt als Biologie)
- Bioanalyse von Nukleinsäuren
Kymos Italien
Pharmaprogress srl wurde 1999 von einem ehemaligen Manager der Angelini-Gruppe gegründet und nahm 2001 den Betrieb als CRO auf. In Camerata Picena, in der Nähe von Ancona, wurde ein 700 m² großes, zweckmäßiges Labor errichtet, das von den italienischen Gesundheitsbehörden GMP-zertifiziert wurde.
Später im Jahr 2023 wurden die Einrichtungen nach Monsano verlegt, wo ein neues Labor mit einer Fläche von 1800 m² gebaut und im darauffolgenden Jahr eingeweiht wurde.
- Stabilitäten, analytische Entwicklung und Validierung
- Qualitätskontrolle von kleinen Molekülen (auch bekannt als Qualitäts- und Massenspektrometrie)
Kymos-Niederlassung in Südkorea
Im Jahr 2024 gründete die Kymos Group ein Verbindungsbüro in Seoul, Südkorea, um die Unterstützung für unsere internationalen Kunden in der gesamten Asien-Pazifik-Region (APAC) zu verbessern.
Dieses Büro befindet sich im renommierten ASEM Tower und dient als unser primärer Ansprechpartner für Pharma- und Biotechnologieunternehmen, die in der Region tätig sind.
ÜBER UNS
Unser Engagement und unser Erfolg
Kymos möchte mehr sein als nur ein Dienstleister; wir wollen ein verlässlicher Partner sein: Wir setzen uns voll und ganz für die Ziele unserer Kunden und die uns anvertrauten Projekte ein; wir liefern qualitativ hochwertige Dienstleistungen zu fairen Preisen, um die Wettbewerbsfähigkeit unserer Kunden zu sichern; wir halten Termine ein, denn die Markteinführungszeit ist ein Schlüsselelement für den Erfolg; und wir engagieren uns ständig in Forschung und Entwicklung, denn nur so können wir den neuen Herausforderungen eines sich schnell verändernden Geschäftsumfelds begegnen.
Dank der Implementierung neuer Dienstleistungen und Funktionen wachsen wir kontinuierlich im zweistelligen Prozentbereich.
Wir sind stolz darauf, jedes Jahr einen sehr hohen Prozentsatz an Stammkunden zu haben.
Wir verzeichnen eine hohe Quote an genehmigten Angeboten, was unser gleichbleibend hohes Qualitätsniveau und faire Preise widerspiegelt.
Der Anteil neuer Kunden steigt von Jahr zu Jahr, vor allem aufgrund unserer Internationalisierungsbemühungen.
Von der Vision zum Wachstum
Unsere Geschichte
Kymos SL wurde 2001 von einem Team aus F&E-Wissenschaftlern mit jahrzehntelanger Erfahrung in der pharmazeutischen Entwicklung gegründet – von der Grundlagenforschung über die finale Formulierung bis hin zu Scale-up-Studien für die Kommerzialisierung. Das Unternehmen nahm seinen Sitz im Wissenschaftspark Barcelona und expandierte trotz starker Konkurrenz rasant. 2011 übernahm Kymos das Immunologie-Team von Ipsen Pharma und schuf damit eine wegweisende Biologika-Abteilung. 2015 bezog Kymos ein brandneues Labor im Technologiepark Vallès. 2016 akquirierte Kymos das italienische Auftragsforschungsinstitut Pharmaprogress. Aufgrund des stetigen Wachstums wurden 2018 zwei aufeinanderfolgende Erweiterungen mit einem neuen Bürogebäude und Laboren notwendig. 2020 übernahm Kymos das deutsche Auftragsforschungsinstitut Proytic. 2021 besteht die Kymos-Gruppe aus einem Hauptsitz mit zwei Gebäuden, zwei europäischen Standorten, 14 Laborabteilungen, 170 hochqualifizierten Experten und 5.000 m² Anlagenfläche mit modernster Ausstattung. In den Jahren 2023-2024 wurde unser italienischer Standort um ein neues Gebäude erweitert, und in Spanien wurde mit dem Bau einer Laborerweiterung begonnen.

Pharmaprogress begann 2001 als Auftragsforschungsinstitut (CRO) für Dritte tätig zu werden, obwohl das Unternehmen bereits 1999 gegründet worden war. In Camerata Picena bei Ancona wurde ein 700 m² großes, speziell dafür eingerichtetes Labor errichtet, das von den italienischen Gesundheitsbehörden nach GLP-Standard zugelassen wurde. Das Unternehmen wurde von einem ehemaligen Manager eines italienischen Pharmaunternehmens gegründet.

Prolytic wurde gegründet. Die Wurzeln der Prolytic GmbH reichen zurück bis zur Viatris GmbH & Co. KG, einem Teil der ASTA Medica AG, einem pharmazeutischen Forschungsunternehmen und ehemals hundertprozentigen Tochterunternehmen der Degussa AG. Die Viatris GmbH & Co. KG wurde an einen Finanzinvestor verkauft, der die Bereiche „Bioanalytik“ und „Pharmakokinetik“ der Arzneimittelentwicklung schloss. Ein erfahrenes Wissenschaftlerteam aus diesen Bereichen gründete im Dezember 2002 die Prolytic GmbH mit dem Ziel, ihre umfassende Expertise in Bioanalytik und Pharmakokinetik Kunden der pharmazeutischen Industrie anzubieten.

Kymos erhielt die GLP-Zertifizierung im Jahr 2002, ganz am Anfang. Die ersten Projekte befassten sich mit Stoffwechsel und Bioanalytik.

Prolytic wurde vom Regierungspräsidium Darmstadt in den Kategorien 1 und 8 GLP-zertifiziert.
Kategorie 1: Physikalische und chemische Eigenschaften und Bestimmung des Gehalts
Kategorie 8: Analytische Untersuchungen an biologischen Materialien

Pharmaprogress wurde im Januar 2009 von der italienischen Arzneimittelbehörde (AIFA) für chemische und physikalische Prüfungen nach GMP-Standard zugelassen.
Die letzte Genehmigung ist Nr. aM-119/2016 vom 22. Juli 2016 und betrifft folgende Prüfungen an Humanarzneimitteln:
1.6.3 Chemische und physikalische Prüfungen gemäß GMP-Qualitätsrichtlinien
1.6.3 Chemische und physikalische GMP-Qualitätskontrolle von Prüfpräparaten

Im Jahr 2009 erhielt das Unternehmen die GMP- und Herstellerzulassung (teilweise Herstellerzulassung für Qualitätskontrollaktivitäten). Ab diesem Zeitpunkt stellte Kymos alle CMC-Aktivitäten (hauptsächlich analytische Entwicklung und Stabilitätsstudien) auf das GMP-Qualitätssystem um und begann mit der Bereitstellung von Qualitätskontrolldienstleistungen für Wirkstoffe und Arzneimittel.

Im Jahr 2011 errichtete Kymos ein mikrobiologisches Labor und erweiterte seine GMP-Zertifizierung auf die mikrobiologische Prüfung nicht steriler Produkte. Diese Zertifizierung wurde 2016 auf sterile Produkte ausgedehnt.

Im Januar 2012 schloss Kymos eine Vereinbarung zur Übernahme der Immunologieabteilung eines ehemaligen Forschungs- und Entwicklungszentrums des französischen multinationalen Konzerns IPSEN in Barcelona. Dank dieser Vereinbarung konnte Kymos eine neue Abteilung für Biologika aufbauen. Erfahrene Mitarbeiter, Geräte und Know-how wurden an Kymos übertragen, und beide Unternehmen unterzeichneten einen langfristigen Kooperationsvertrag zur gemeinsamen Entwicklung innovativer Medikamente.

Im Januar 2015 verlegte das Unternehmen seinen Firmensitz von Barcelona (Barcelona Science Park) in ein freistehendes Gebäude in Cerdanyola del Vallès (Vallès Technology Park). Ein brandneues Labor wurde errichtet, wodurch sich die Fläche von 650 m² auf 1.500 m² vergrößerte. Dies ermöglichte es dem Unternehmen, seinen Umsatz zu steigern und die Belegschaft in den Jahren 2015 und 2016 zu vergrößern. Im selben Jahr erhielt Kymos die Einfuhrgenehmigung für Arzneimittel. Zudem wurden Chargenfreigabeverfahren für die Vermarktung von Produkten eingeführt.

Im November 2016 übernahm das Unternehmen das italienische Auftragsforschungsinstitut Pharmaprogress. Das Unternehmen mit Sitz in Ancona beschäftigte acht Mitarbeiter und verfügte über 700 m² Laborfläche für die Bioanalytik und die analytische Entwicklung von Wirkstoffen und Arzneimitteln. Mittlerweile ist Pharmaprogress vollständig in Kymos integriert und beschäftigt 16 Mitarbeiter.

Im Juli wurde Kymos einer allgemeinen Standortinspektion durch die FDA unterzogen. Die Inspektion wurde erfolgreich abgeschlossen und der entsprechende Umweltverträglichkeitsbericht (EIR) wurde ausgestellt.

Im Juli erweiterte Kymos seine Räumlichkeiten und zog in ein neues, freistehendes Gebäude in der Nähe des bestehenden um. Dieses neue Gebäude verfügt über einen Schulungsraum, ein Archiv, verschiedene Besprechungsräume und eine Cafeteria.

Im August zog Prolytic in größere und hochmoderne Räumlichkeiten in der Weismüllerstraße 45 um. Das 15-köpfige Team verdoppelte seine Größe und verfügt nun über 800 m² Labor- und Bürofläche, um seinen Kunden die besten bioanalytischen und pharmakokinetischen Dienstleistungen anbieten zu können.

Im April schloss die FDA die Inspektion des Pharmaprogrees-Standorts in Ancona ab und bestätigte, dass dieser für die Zulassung von Arzneimitteln in den USA geeignet ist. Es handelte sich um eine Dokumentenprüfung, die auf der vorherigen Inspektion der italienischen Arzneimittelbehörde AIFA (Agenzie Italiana del Farmaco) basierte, dank des neuen Abkommens über die gegenseitige Anerkennung zwischen der EMA und der FDA.

Im Mai erweiterte Kymos seine Einrichtungen erneut um neue Labore für analytische Entwicklung und biopharmazeutische Tests. Im Laufe des Jahres trugen Chargenprüfungen für Biosimilars und asiatische Kunden maßgeblich zum Unternehmenswachstum bei.

Im Oktober 2020 fusionierte Kymos mit dem deutschen bioanalytischen Labor Prolytic GmbH mit Sitz in Frankfurt am Main. Prolytic beschäftigte 16 Mitarbeiter und war auf die Bioanalyse von kleinen und großen Molekülen sowie Oligonukleotiden und Pharmakokinetik spezialisiert.

Kymos ist ein sehr international ausgerichtetes Unternehmen. Neben unseren drei Standorten in verschiedenen europäischen Ländern betreuen wir Kunden weltweit. Im Jahr 2021 haben wir erstmals die Marke von 40 Ländern überschritten, in denen unsere Kunden auf allen Kontinenten vertreten sind.
2022 erwarb Kymos ein geräumigeres, komfortableres und moderneres Gebäude in der Region Ancona. Teile des Gebäudes müssen renoviert werden, und es liegt noch viel Arbeit vor uns. Doch im nächsten Jahr kann Pharmaprogress endlich in die neuen, modernen Räumlichkeiten umziehen.

Kymos erhielt die offizielle Zertifizierung der ANVISA (Agència Nacional de Vigilància Sanitária) für Bioäquivalenzstudien und die Genehmigung zur Teilnahme an diesen Studien für die Einreichung in Brasilien. Die Arbeiten am neuen Gebäude von Pharmaprogress sind abgeschlossen und wir haben mit dem Umzug begonnen.

Unser neues Gebäude (1800 m²) in Italien wurde Anfang des Jahres offiziell eingeweiht, und alle Geräte und Projekte wurden an unseren neuen Standort in Monsano verlegt. Die Arbeiten an der Laborerweiterung in Spanien (+600 m²) haben begonnen.

Nehmen Sie Kontakt mit uns auf